Genética
- Gen: Es todo segmento de ADN(Ácidodesoxiribonucléico) que contiene varias características.
- Alelo: Es una característica específica.
- Qué es la genética?
- Gen dominante:
presente una forma distinta del gen en el cromosoma
homólogo. Se escribe o representa con letra mayúscula.
- Gen dominante:
- Referente histórico de la genética:
Gregor Mendel,llamado el padre de la genética creó dos leyes llamadas, La ley de la segregación y La ley de caracteres independientes.
- Ley de la segregación:
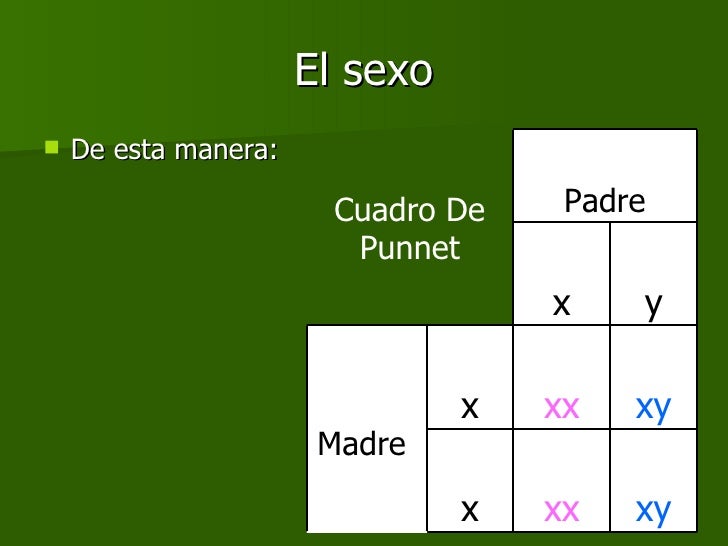
Esta ley establece que durante la formación de los Gametos, cada alelo de un par se separa del otro miembro para determinar la constitución genética del gameto filial. Es muy habitual representar las posibilidades de hibridación mediante cuadro de Punnett.
De acuerso a esta ley, en la planta se podían encontrar en cuatro partes de la planta siete caracteres, como:
En la semilla se podían diferenciar el color de los cotiledones y la forma de esta.
En las flores se podía diferenciar el color de cada una.
En la vaina/fruto se podía diferenciar su tipo, si era lisa o arrugada y su color.
Finalmente, en el tallo se podía diferenciar su longitud y la posición.
- Ley de caracteres independientes:
se hace referencia al caso de que se contemplen dos caracteres distintos. Cada uno de ellos se transmite siguiendo de manera independiente las leyes anteriores, como si no existiera presencia del otro carácter.
- Proceso de sus experimentos:
Mendel comenzó sus experimentos con el guisante común o arveja; abundante, fácil de cultivar, cruces en poco tiempo permitiendo ver cambios de generación de en generación, es una de la razones del porque escogió este tipo de planta.
Esta también hace autopolinización.
Mendel concluyó que las características heredadas son llevadas por factores individuales conocidos hoy en día como genes.
Al momento en el que salían los cruces, si en la primera generación toda la progenie mostraba solo una de las dos características se le denominaba Dominante.
Al autopolinizarse las plantas, Mendel encontró que en la segunda generación había tres caracteres dominantes y uno recesivo.
Si los dos alelos son iguales el organismo es homocigoto para esa característica. Si los dos alelos son diferentes el organismo es heterocigoto para las características.
Ahora unos ejemplos de tabla de punnett:
Referencias Bibliográficas:
http://www.mendel.es/leyes-de-mendel
http://datateca.unad.edu.co/contenidos/201101/curso/leyesherencia.html
http://www.unav.es/ocw/genetica/tema11-2.html
http://es.slideshare.net/profesorleonardo/serie-ciencias-naturales-17-e
Ahora unos ejemplos de tabla de punnett:
Referencias Bibliográficas:
http://www.mendel.es/leyes-de-mendel
http://datateca.unad.edu.co/contenidos/201101/curso/leyesherencia.html
http://www.unav.es/ocw/genetica/tema11-2.html
http://es.slideshare.net/profesorleonardo/serie-ciencias-naturales-17-e